Comme de nombreux Sponsors peuvent en témoigner, la préparation de l'ensemble des données conformes au CDISC est longue et coûteuse. Il est important de prendre en compte les réglementations actuelles et futures sur les données lors de la planification des études pour votre programme de développement.
Le domaine PC, contenant les concentrations PK, et le domaine PP, contenant les données des paramètres PK calculées par les scientifiques PK, sont deux exemples de domaines SDTM clés pour les analyses PK et la pharmacométrie.
Chez PhInc. Modeling, nous comprenons que l'utilisation des normes CDISC peut représenter un coût supplémentaire, mais ces normes ont également de nombreux avantages pour le sponsor :
- Normalisation de l'analyse et de la communication des données
- Faciliter la mise en commun des données pour de futures analyses telles que la modélisation de la population PK
- Facilitation de l'examen des données des études par les régulateurs
- Amélioration de la transférabilité des résultats des études (y compris PK)
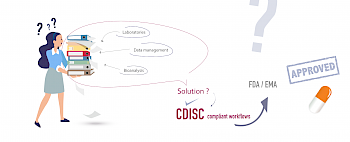
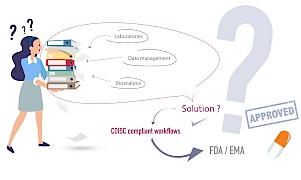
 Un exemple de flux de travail incorporant des ensembles de données SDTM dans un PK conforme à CDISC typique est illustré sur le schéma ci-contre.
Un exemple de flux de travail incorporant des ensembles de données SDTM dans un PK conforme à CDISC typique est illustré sur le schéma ci-contre.
Implémentation des standards PK CDISC
Le principal défi est d'abord de coordonner efficacement avec toutes les parties prenantes du processus CDISC : gestion des données, bioanalyse et soumission réglementaire.
C'est pour cela que nous suggérons toujours d'impliquer PK expérimenté scientifiques au début du processus, pour assurer une bonne communication entre les acteurs et éviter d'avoir différentes équipes travaillant en vase clos (en silos).
Comment PhInc. Modeling peut vous aider !
- En impliquant des pharmacométriciens et des experts en PK dans le processus de transfert de données, ainsi que dans le jeu de données d'analyse création. PhInc. Modeling garantit que les données transférées comprennent tous les éléments essentiels nécessaires à la réalisation des analyses / modélisation. Cela réduit les délais après le début de l'analyse en réduisant les allers-retours et augmente la conformité au normes CDISC. Par exemple, nous avons observé que très peu d'équipes CDISC / de gestion des données traitent les ressources internes pour assurer la livraison d'ensembles de données PK de haute qualité au format CDISC, en particulier pour les Etudes PK.
- En utilisant un processus CDISC natif pour les analyses PK, nous garantissons la livraison transparente de résultats conformes au CDISC qui sont facilement reproductibles et prennent en compte tous les aspects de l'analyse. Tant la source (bioanalyse), les données et les résultats d'analyse (pharmacocinétique) sont générés directement au format CDISC par opposition à l'approche alternative consistant à convertir rétroactivement les données en un format CDISC (mapping), un processus qui est sujettes à des erreurs et peuvent réduire la valeur de réutilisabilité des résultats PK.
N'hésitez pas à vous mettre en contact avec nos experts CDISC ! Ils sont là pour répondre à toutes vos interrogations. CONTACTEZ-NOUS